Зовнішнє незалежне оцінювання 2012 року з хімії
2. Частка від ділення середньої молярної маси повітря на молярний об’єм газів (н. у.) - це
3. Яке твердження щодо положення хімічних елементів у періодичній системі Д.І. Менделєєва правильне?
7. Проаналізуйте твердження й укажіть правильні.
I. Швидкість хімічної реакції зростає внаслідок подрібнення реагентів.
II. Швидкість хімічної реакції зростає внаслідок збільшення концентрації реагентів.
I. Швидкість хімічної реакції зростає внаслідок подрібнення реагентів.
II. Швидкість хімічної реакції зростає внаслідок збільшення концентрації реагентів.
8. Що спостерігатиме учень, який до розбавленого водного розчину калій гідроксиду, підфарбованого фенолфталеїном, поступово добавлятиме хлоридну кислоту?
9. Укажіть кількість речовини (моль) катіонів, що утворилися внаслідок електролітичної дисоціації в розбавленому водному розчині натрій сульфату кількістю речовини З моль.
10. Проаналізуйте твердження й укажіть правильні.
І Розчинність газів у воді зростає внаслідок підвищення тиску.
II. Розчинність газів у воді зменшується внаслідок підвищення температури
І Розчинність газів у воді зростає внаслідок підвищення тиску.
II. Розчинність газів у воді зменшується внаслідок підвищення температури
12. Які властивості виявляє купрум(ІІ) гідроксид?
1. за нагрівання розкладається
2. реагує із хлоридною кислотою
3. легко окиснюється
4. є сильним електролітом
1. за нагрівання розкладається
2. реагує із хлоридною кислотою
3. легко окиснюється
4. є сильним електролітом
14. Які твердження щодо способів пом’якшення води правильні?
1. постійну твердість води усувають кип’ятінням
2. тимчасову твердість води усувають добавлянням кальцій гідроксиду
3. тимчасову твердість води усувають кип’ятінням
4. постійну твердість води усувають добавлянням натрій сульфату
1. постійну твердість води усувають кип’ятінням
2. тимчасову твердість води усувають добавлянням кальцій гідроксиду
3. тимчасову твердість води усувають кип’ятінням
4. постійну твердість води усувають добавлянням натрій сульфату
15. Які схеми відображають амфотерні властивості речовини?
1. Al0 + H+ → Al3+ + H2
2. Al3+ + OH- → Al(OH)3
3. Al2O3 + H+ → Al3+ + H2O
4. Al2O3 + OH- → AlO-2 + H2O
1. Al0 + H+ → Al3+ + H2
2. Al3+ + OH- → Al(OH)3
3. Al2O3 + H+ → Al3+ + H2O
4. Al2O3 + OH- → AlO-2 + H2O
19. Перетворіть запис Al + HCl →... на хімічне рівняння та вкажіть суму коефіцієнтів у ньому.
21. Які речовини використовують для добування гідроген хлориду в промисловості?
23. Укажіть суму коефіцієнтів у правій частині рівняння реакції термічного розкладання купрум(ІІ) нітрату.
26. Які твердження щодо членів одного гомологічного ряду правильні?
1 група атомів СН2 - це гомологічна різниця
2 гомологи мають однаковий кількісний склад
3 гомологи мають однаковий якісний склад
4 гомологи мають однакові температури кипіння
1 група атомів СН2 - це гомологічна різниця
2 гомологи мають однаковий кількісний склад
3 гомологи мають однаковий якісний склад
4 гомологи мають однакові температури кипіння
30. Проаналізуйте твердження й укажіте привильні.
I. Бензен знебарвлює бромну воду.
II. Бензен можна добути тримеризацією етану.
I. Бензен знебарвлює бромну воду.
II. Бензен можна добути тримеризацією етану.
37. Який об’єм (л) кисню витратиться під час згоряння метиламіну об’ємом 4 л (об’єми газів виміряно за однакових умов)?
38. Укажіть колір нітрогеновмісних сполук, які утворюються внаслідок добавляння концентрованої нітратної кислоти до білка.
39. Яку речовину застосовують як мономер для добування полібутадієнового каучуку?
41. Установіть відповідність між схемами та типами хімічних реакції
| 1. ZnO + HCl → ZnCl2 + H2O 2. SO3 + H2O → H2SO4 3. Zn + H2SO4 → ZnSO4 + H2 4. Al(OH)3 → AL2O3 + H2O | А. обміну Б. заміщення В. розкладу Г. сполучення Д. дегідрування |
42. Установіть відповідність між формулами та природою речовини.
| 1. SO2 2. KOH 3. H2S 4. Na2SO3 | А. луг Б. кислотний оксид В. сіль Г. одноосновна кислота Д. двоосновна кислота |
43. Установіть відповідність між структурними формулами речовин і префіксами в їхніх назвах.
1. 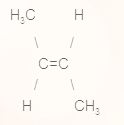 2. 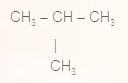 3. 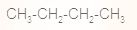 4. 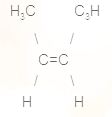 | А. цикло Б. н- В. цис Г. ізо Д. транс- |
44. Укажіть відповідність між хімічними формулами та природою речовини
1. 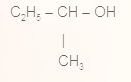 2. 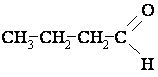 3. 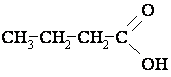 4. 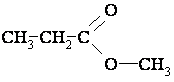 | А. спирт Б. альдегід В. естер Г. етер Д. кислота |
45. Розташуйте хімічні елементи за збільшенням числа електронів на зовнішньому енергетичному рівні їхніх атомів.
А. F
Б. Al
В. S
Г. Li
А. F
Б. Al
В. S
Г. Li
46. Розташуйте хімічні елементи за зменшенням радіусів атомів
А. Al
Б. Mg
В. Si
Г. C
А. Al
Б. Mg
В. Si
Г. C
47. Установіть послідовність хімічних формул речовин у ланцюжку перетворень неметалу на кислу сіль.
А. Na3PO4
Б. NaH2PO4
В. P
Г. P2O5
А. Na3PO4
Б. NaH2PO4
В. P
Г. P2O5
48. Установіть послідовність хімічних формул речовин у ланцюжку перетворень гідроксиду на сіль.
А. FeCl2
Б. Fe2O3
В. Fe(OH)3
Г. Fe
А. FeCl2
Б. Fe2O3
В. Fe(OH)3
Г. Fe
49. Установіть послідовність хімічних формул речовин у ланцюжку перетворень неорганічної речовини на естер.
А. HCOOH
Б. CH3OH
В. CO
Г. HCOOCH3
А. HCOOH
Б. CH3OH
В. CO
Г. HCOOCH3
50. Установіть послідовність хімічних формул речовин у ланцюжку перетворень дисахариду на альдегід.
А. C6H12O6
Б. C2H4O
В. C12H22O11
Г. C2H6O
А. C6H12O6
Б. C2H4O
В. C12H22O11
Г. C2H6O
52. Обчисліть масу осаду, що утвориться внаслідок змішування двох водних розчинів, один з яких містить магній нітрат кількістю речовини 0,5 моль, а інший - натрій карбонат масою 56г.
53. Використовуючи метод електронного балансу перетворіть схему реакції
Mg + HNO3(роз.) → Mg(NO3)2 + NH4NO3 + H2O
на хімічне рівняння і вкажіть коефіцієнт перед формулою окисника.
Mg + HNO3(роз.) → Mg(NO3)2 + NH4NO3 + H2O
на хімічне рівняння і вкажіть коефіцієнт перед формулою окисника.
54. Обчисліть об’єм (мл) води, для виготовлення розчину масою 200г із масовою часткою натрій нітрату 0,25.
55. На суміш порошків магній сульфату та магній карбонату масою 100г подіяли надлишком хлоридної кислоти. У результаті реакції виділився газ, об’ємом 11,2л (н.у.). Обчисліть масову частку (%) магній карбонату у суміші.
56. Продуктами повного окиснення вуглеводню є карбон(ІV)оксид масою 26,4г і вода масою 5,4г. Відносна густина вуглеводню за воднем дорівнює 39. Укажіть число атомів Карбону в молекулі вуглеводню.
57. Запишіть локанти без розділових знаків послідовно, як вони розташовані за номенклатурою ІЮПАК, у назві речовини, структурна формула якої
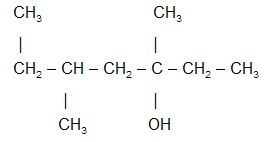
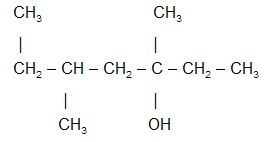
59. Обчисліть об’ємну частку (%) хлору в суміші, що складається з хлору об’ємом 2,5л і кисню об’ємом 7,5л.
60. Обчисліть об’єм (л) кисню, що витратиться на повне окиснення пропену об’ємом 4 л (об’єми газів виміряно за однакових умов).
